HDAC8是一种Zn²⁺依赖型的I类去乙酰化酶HDAC,通过催化粘连蛋白cohesin亚基SMC3去乙酰化,在细胞周期过程中发挥重要作用。HDAC8过表达能够增强多种癌细胞的增殖、转移及抗药性,而其突变会导致多种严重的先天性遗传疾病,例如狄朗热综合征(CdLS)和杜欣氏肌萎缩症(DMD)。尽管目前对HDAC8的结构和功能已有较为深入的研究,但其在细胞周期调控中的具体机制仍有待进一步阐明。
2024年7月,复旦大学余巍组在EMBO Reports在线发表题为“Reversible acetylation of HDAC8 regulates cell cycle”的文章,该研究揭示了HDAC8的可逆乙酰化修饰作为应激响应的关键细胞周期调节因子。
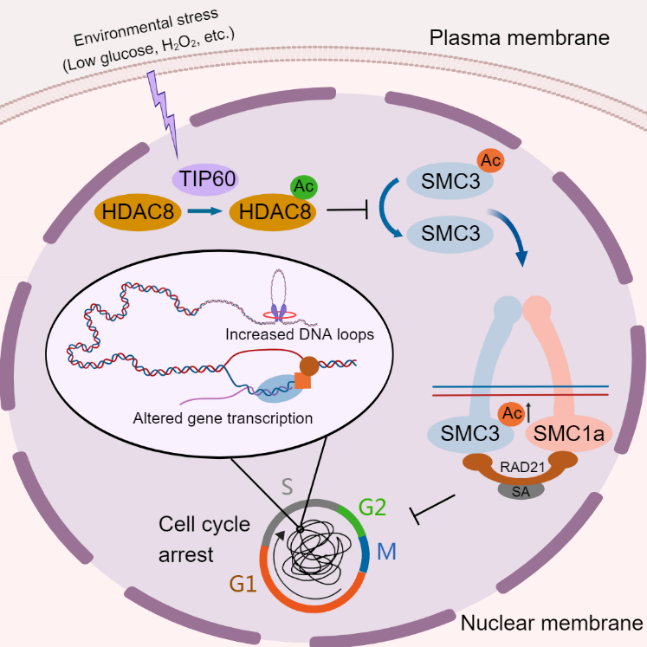
本研究发现HDAC8作为一个去乙酰化酶存在乙酰化修饰,负向调控其酶活,且HDAC8乙酰化水平在细胞周期过程中表现出动态变化。有趣的是,外部环境刺激比如葡萄糖剥夺能够促进乙酰基转移酶Tip60催化HDAC8乙酰化,导致粘连蛋白cohesin亚基SMC3乙酰化水平增加和细胞周期停滞。此外,构建模拟HDAC8乙酰化突变的细胞表现出广泛的基因转录表达变化,这可能与三维基因组结构的改变尤其是染色质环的增强有关。数据还表明,HDAC8乙酰化通过破坏细胞周期相关基因的表达和姐妹染色单体的粘连,负向调控细胞周期进展,导致G2/M期停滞。这些发现阐明HDAC8的可逆乙酰化修饰作为一种新的细胞周期调控因子,拓展了对细胞周期动态调控过程的理解,尤其是应激响应机制。
在这项研究中,课题组构建了表达模拟乙酰化突变的HDAC8-KQ 基因敲入细胞。为了研究3D基因组结构的变化,课题组对经典Hi-C技术进行了简便而有效的改进,应用于难以大量获取的HDAC8-KQ Knock-in细胞,显著减少实验过程中样本DNA的损失。改进后的Hi-C方法能够利用少量细胞生成高分辨率的Hi-C图谱,这有利于拓展了Hi-C技术的应用范围,尤其是为研究稀有临床样本的染色质三维结构提供了方法的支持。
HDAC8在人类病理生理学中发挥着重要功能,较为典型的是其突变可以导致罕见的多系统发育缺陷疾病——狄朗热综合征(CdLS)。本研究首次揭示了HDAC8在调控细胞周期过程中姐妹染色单体内聚以及染色质三维结构的重要角色,暗示CdLS患者细胞中广泛的基因转录缺陷可能与HDAC8介导的染色质三维结构调控密切相关,为CdLS等HDAC8相关疾病的致病机制提供了新的见解。
本研究受到国家自然科学基金和科技部重点研发计划资助。复旦大学研究生桑超伟和李雪东为本文共同第一作者,余巍教授是通讯作者,复旦大学于淼研究员和林金钟教授对该研究提供重要帮助。
http://doi.org/10.1038/s44319-024-00210-w

